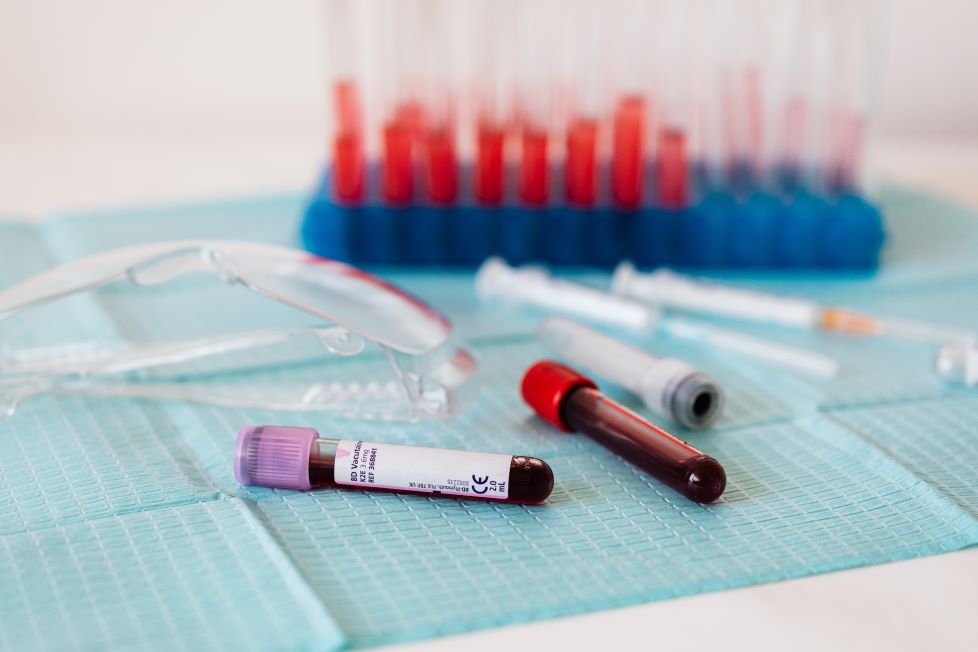
Arrivano misure comuni europee sui test antigenici rapidi
A seguito dell'accordo degli Stati membri su un Quadro comune sull’uso dei test antigenici rapidi, il Comitato per la Sicurezza Sanitaria ha presentato un documento dettagliato in materia. Tra le misure l'introduzione di una lista di test, e un insieme standardizzato di dati per tutti i certificati.